Парсабив (Parsabiv)
💊 Состав препарата Парсабив
✅ Применение препарата Парсабив
Препарат отпускается по рецепту
Входит в список «Жизненно необходимых и важнейших лекарственных
препаратов»
Температура хранения: от 2 до 8 °С
Описание активных компонентов препарата
Парсабив
(Parsabiv)
Приведенная научная информация является обобщающей и не может быть использована для принятия
решения о возможности применения конкретного лекарственного препарата.
Дата обновления: 2022.07.21
Владелец регистрационного удостоверения:
Код ATX:
H05BX04
(Этелкальцетид)
Лекарственная форма
|
Препарат отпускается по рецепту |
Парсабив |
Раствор для внутривенного введения 2.5 мг/0.5 мл: фл. 6 шт. рег. №: ЛП-(003004)-(РГ-RU) |
Форма выпуска, упаковка и состав
препарата Парсабив
Раствор для в/в введения в виде бесцветной, прозрачной жидкости, свободной от механических включений.
Вспомогательные вещества: натрия хлорид — 4.3 мг, янтарная кислота — 0.6 мг, хлористоводородная кислота — до pH 3.3, натрия гидроксид — до pH 3.3 мг, вода д/и — до объема 0.5 мл.
0.5 мл — флаконы объемом 3 мл (6) — упаковки ячейковые контурные (1) — пачки картонныех.
х на пачку наклеивают одну прозрачную защитную этикетку для контроля первого вскрытия.
Фармакологическое действие
Антипаратиреоидное средство, кальцимиметик, синтетический пептид. Этелкальцетид специфически связывается с кальций-чувствительными рецепторами (CaSR) и вызывает их активацию, что приводит к снижению секреции паратиреоидного гормона (ПТГ) главными клетками паращитовидной железы.
У пациентов, находящихся на гемодиализе, снижение концентрации ПТГ коррелирует с концентрацией этелкальцетида в плазме крови. Уменьшение концентрации ПТГ ассоциируется с сопутствующим снижением концентраций кальция и фосфатов в сыворотке крови.
После однократного в/в болюсного введения этелкальцетида происходит быстрое (в течение 30 мин) снижение концентрации ПТГ. Выраженность и продолжительность снижения ПТГ усиливаются с увеличением дозы. Снижение концентрации ПТГ ведет к снижению концентрации кальция и ограничивает увеличение концентрации фосфатов после диализа. При в/в болюсном введении этелкальцетида 3 раза в неделю снижение концентрации ПТГ сохранялось в течение 6 месяцев.
Фармакокинетика
У пациентов с хронической почечной недостаточностью и вторичным гиперпаратиреозом, которым требуется проведение гемодиализа, фармакокинетика этелкальцетида характеризовалась линейностью и не изменялась с течением времени как после в/в введения однократной дозы (5-60 мг), так и после в/в введения повторных доз (2.5-20 мг). После в/в введения кинетика этелкальцетида демонстрировала триэкспоненциальный спад. На фоне в/в введения 3 раза в неделю в конце 3-4 ч процедуры гемодиализа концентрации этелкальцетида в плазме крови достигали практически равновесного состояния у пациентов с ХПН спустя 4 недели после начала лечения, при этом наблюдаемая кумуляция увеличивалась в 2-3 раза, а эффективный период полувыведения составлял 3-5 дней. У пациентов с нормальной функцией почек происходит быстрое выведение этелкальцетида, в то время как у пациентов с ХПН. которым требуется проведение гемодиализа, гемодиализ становится основным путем элиминации препарата.
В популяционной фармакокинетической модели Vss составлял приблизительно 796 л. Этелкальцетид преимущественно связывается с альбумином сыворотки крови посредством обратимого ковалентного связывания. Способность к нековалентному связыванию у этелкальцетида низкая, а коэффициент несвязанной фракции составляет 0.53. Соотношение между концентрациями [14С]-этелкальцетида в крови и в плазме крови составляет примерно 0.6.
В крови этелкальцетид подвергается биотрансформации посредством обратимого дисульфидного обмена с эндогенными тиолами с преимущественным образованием конъюгатов с сывороточным альбумином.
Экспозиция продуктов биотрансформации в плазме крови была приблизительно в 5 раз выше, чем экспозиция этелкальцетида, а профиль концентрация-время продуктов биотрансформации был сопоставим с профилем этелкальцетида.
У пациентов с хронической почечной недостаточностью, которым требовалось проведение гемодиализа, гемодиализ становился основным путем элиминации этелкальцетида. Эффективное выведение этелкальцетида происходило при клиренсе гемодиализа 7.66 л/ч. После введения одной дозы этелкальцетида, меченного радиоактивным изотопом, пациентам с ХПН и вторичным ГПТ, которым требовалось проведение гемодиализа, в диализате обнаружено примерно 60% [14С]-этелкальцетида, а суммарно в моче и кале — 7% в течение 175 дней периода сбора.
Показания активных веществ препарата
Парсабив
Лечение вторичного гиперпаратиреоза у пациентов с хронической почечной недостаточностью, находящихся на гемодиализе.
Режим дозирования
Способ применения и режим дозирования конкретного препарата зависят от его формы выпуска и других факторов. Оптимальный режим дозирования определяет врач. Следует строго соблюдать соответствие используемой лекарственной формы конкретного препарата показаниям к применению и режиму дозирования.
Вводят болюсно 3 раза в неделю.
Введение проводят через венозный катетер диализной системы в период промывки в конце процедуры гемодиализа, либо внутривенно после промывки катетера.
Перед введением первой дозы этелкальцетида, увеличением дозы или повторного применения после временного прекращения лечения концентрация альбумин-корригированного кальция в сыворотке крови должна составлять ≥8.3 мг/дл.
Рекомендуемая начальная доза — 5 мг.
Дозу следует подбирать индивидуально в диапазоне от 2.5 до 15 мг.
В случае клинически значимого снижения концентрации альбумин-корригированного кальция в сыворотке крови ниже 8.3 мг/дл и/или появления симптомов гипокальциемии проводится коррекция лечения по специальной схеме.
Побочное действие
Со стороны обмена веществ: очень часто — снижение концентрации кальция в крови; часто — гипокальциемия, гиперкалиемия, гипофосфатемия.
Со стороны нервной системы: часто — головная боль, парестезии.
Со стороны сердечно-сосудистой системы: часто — декомпенсация хронической сердечной недостаточности, артериальная гипотензия.
Со стороны пищеварительной системы: очень часто — тошнота, рвота, диарея.
Со стороны костно-мышечной системы: очень часто — мышечные спазмы; часто — миалгия.
Противопоказания к применению
Гипокальциемия (концентрация альбумин-корригированного кальция в сыворотке крови ниже нижнего предела нормальных значений), беременность, период грудного вскармливания, возраст до 18 лет, повышенная чувствительность к этелкальцетиду.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Применение при нарушениях функции печени
Препарат разрешен для применения при нарушении функции печени
Применение при нарушениях функции почек
Предназначен для применения у пациентов, находящихся на гемодиализе.
Применение у детей
Препарат противопоказан для применения у детей и подростков в возрасте до 18 лет
Особые указания
Этелкальцетид снижает сывороточную концентрацию кальция и может привести к развитию гипокальциемии.
Следует наблюдать за пациентом для выявления гипокальциемии. Контроль концентрации кальция в сыворотке крови следует осуществлять перед началом терапии, в течение одной недели после начала терапии или коррекции дозы, а также каждые 4 недели лечения этелкальцетидом. Возможные клинические проявления гипокальциемии включают парестезии, миалгии, мышечные спазмы и судороги. Пациенту следует рекомендовать обратиться к врачу в случае появления симптомов гипокальциемии. При клинически значимом снижении концентрации альбумин-корригированного кальция в сыворотке крови необходимо провести мероприятия, направленные на повышение концентрации кальция в сыворотке.
Снижение концентрации кальция в сыворотке крови может привести к удлинению интервала QT, что, в свою очередь, может сопровождаться развитием желудочковой аритмии. У пациентов с врожденным синдромом удлинения интервала QT, удлинением интервала QT в анамнезе, удлинением интервала QT или внезапной сердечной смертью в семейном анамнезе, а также другими состояниями-предикторами удлинения интервала QT и развития желудочковой аритмии необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения.
Порог судорожной готовности может быть снижен при значительном уменьшении концентрации кальция в сыворотке крови. У пациентов с судорожными расстройствами в анамнезе необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения.
Снижение функции миокарда, артериальная гипотензия и хроническая сердечная недостаточность могут быть связаны со значительным уменьшением концентрации кальция в сыворотке крови. У пациентов с хронической сердечной недостаточностью в анамнезе (которая может ассоциироваться с уменьшением концентрации кальция в сыворотке крови) необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения.
Пациентам, получающим этелкальцетид не следует назначать цинакальцет. Их одновременное применение может привести к развитию тяжелой гипокальциемии.
С осторожностью применять у пациентов, получающих любые другие лекарственные средства, снижающие концентрацию кальция в сыворотке крови. В таких случаях необходимо тщательно контролировать концентрацию кальция в крови.
При длительном подавлении концентрации ПТГ ниже 100 пг/мл возможно развитие адинамической болезни кости. При снижении концентрации ПТГ ниже рекомендуемого целевого диапазона необходимо уменьшить дозы или отменить терапию стероловыми формами витамина D и/или этелкальцетидом. После отмены терапию возобновляют в более низких дозах для поддержания концентрации ПТГ’ в пределах диапазона целевых значений.
Не отмечено изменения фармакокинетического профиля, клинического ответа или профиля безопасности, вызванных наличием антител к этелкальцетиду, изначально присутствовавших, или выработанных во время лечения.
Лекарственное взаимодействие
Одновременное применение других лекарственных средств, снижающих концентрацию кальция в сыворотке крови, и этелкальцетида может привести к повышению риска развития гипокальциемии.
Адрес производителя
|
PATHEON MANUFACTURING SERVICES , LLC |
США |
5900 Martin Luther King Jr. Highway, Greenville, North Carolina, 27834, USA |
|
AMGEN MANUFACTURING , Limited |
Пуэрто-Рико |
Road 31, Km 24.6, Juncos 00777, Puerto Rico, USA |
Если вы хотите разместить ссылку на описание этого препарата — используйте данный код
Парсабив — инструкция по применению
Синонимы, аналоги
Статьи
Регистрационный номер:
ЛП 003993 — 051216
Торговое наименование:
Парсабив
Международное непатентованное название:
этелкальцетид
Форма выпуска:
раствор для внутривенного введения
СОСТАВ
Один флакон 0,5 мл содержит:
Действующее вещество: 3.1 мг этелкальцетида гидрохлорида (2,5 мг в пересчете на этелкальцетид) в 0,5 мл раствора (5 мг/мл)
Вспомогательные вещества: натрия хлорид — 4,3 мг, янтарная кислота -0,6мг, хлористоводородная кислота — до рН 3,3, натрия гидроксид — до рН 3,3, вода для инъекций — до объема 0,5 мл
Один флакон 1,0 мл содержит
Действующее вещество:
6.2 мг этелкальцетида гидрохлорида (5 мг в пересчете на этелкальцетид) в 1 мл раствора (5 мг/мл)
Вспомогательные вещества: натрия хлорид — 8,5 мг, янтарная кислота — 1,2 мг, хлористоводородная кислота — до рН 3,3, натрия гидроксид — до рН 3,3, вода для инъекций — до объема 1,0 мл
Один флакон 2,0 мл содержит
Действующее вещество:
12,3 мг этелкальцетида гидрохлорида (10 мг в пересчете на этелкальцетид) в 2 мл раствора (5 мг/мл)
Вспомогательные вещества: натрия хлорид — 17,0 мг, янтарная кислота -2,4 мг, хлористоводородная кислота — до рН 3,3, натрия гидроксид — до рН 3,3, вода для инъекций — до объема 2,0 мл
ОПИСАНИЕ
Прозрачная бесцветная жидкость, свободная от механических включений.
ФАРМАКОТЕРАПЕВТИЧЕСКАЯ ГРУППА
Антипаратиреоидное средство
Код ATX: Н05ВХ04
ФАРМАКОЛОГИЧЕСКИЕ СВОЙСТВА
Фармакодинамика
Механизм действия
Этелкальцетид представляет собой синтетический пептид, кальцимиметик. Этелкальцетид специфически связывается с кальций-чувствительными рецепторами (CaSR) и вызывает их активацию, что приводит к снижению секреции паратиреоидного гормона (ПТГ) главными клетками паращитовидной железы. У пациентов, находящихся на гемодиализе, снижение концентрации ПТГ коррелирует с концентрацией этелкальцетида в плазме крови. Уменьшение концентрации ПТГ ассоциируется с сопутствующим снижением концентраций кальция и фосфатов в сыворотке крови.
После однократного внутривенного (в/в) болюсного введения этелкальцетида происходит быстрое (в течение 30 минут) снижение концентрации ПТГ. Выраженность и продолжительность снижения ПТГ усиливаются с увеличением дозы. Снижение концентрации ПТГ ведет к снижению концентрации кальция и ограничивает увеличение концентрации фосфатов после диализа. При в/в болюсном введении этелкальцетида 3 раза в неделю снижение концентрации ПТГ сохранялось в течение 6 месяцев.
Данные клинических исследований
Оценка препарата Парсабив проводилась в трех 6-месячных многоцентровых рандомизированных двойных-слепых контролируемых клинических исследованиях у пациентов с вторичным гиперпаратиреозом (ГПТ) при хронической почечной недостаточности (ХПН). находящихся на гемодиализе. Изучение препарата Парсабив также проводилось в рамках одного многоцентрового неконтролируемого исследования по оценке безопасности перевода пациентов с вторичным ГПТ, находившихся на гемодиализе, с перорального приема цинакальцета на в/в введение препарата Парсабив.
Эффективность и безопасность препарата Парсабив у пациентов с вторичным ГПТ с ХПН. находившихся на гемодиализе 3 раза в неделю, оценивались в двух 6-месячных многоцентровых рандомизированных двойных-слепых плацебо-контролируемых исследованиях. В каждом из исследований первичная конечная точка была представлена долей пациентов, достигших на протяжении периода оценки эффективности (ЕАР) снижения концентрации ПТГ более чем на 30% по сравнению с исходным значением. Вторичные конечные точки были представлены долей пациентов со средним уровнем ПТГ < 300 пг/мл во время периода оценки эффективности, процентным изменением относительно исходных уровней во время периода оценки эффективности таких показателей, как концентрация ПТГ. альбумин-корригированного кальция в сыворотке крови, произведения кальций-фосфор (Са х Р).
В данных плацебо-контролируемых исследованиях участвовали в общей сложности 1,023 пациентов (509 получали Парсабив, 514 — плацебо). Демографические и исходные характеристики обеих групп в обоих исследованиях были сопоставимы. В исследованиях были получены схожие результаты: на протяжении периода оценки эффективности препарата Парсабив в сравнении с плацебо статистически значимо увеличивал долю пациентов, у которых происходило снижение средней концентрации ПТГ более чем на 30% относительно исходного значения, увеличивал долю пациентов со средней концентрацией ПТГ < 300 пг/мл (вторичная оценка эффективности), а также вызывал статистически значимое снижение концентрации ПТГ, альбумин-корригированного кальция, фосфатов и произведения кальций-фосфор (Са х Р). Снижение концентрации ПТГ, альбумин-корригированного кальция, фосфатов и Са х Р в сыворотке крови поддерживалось на протяжении 78 недель лечения. Парсабив вызывал снижение концентрации ПТГ независимо от его исходного значения, продолжительности диализа, предшествующего лечения цинакальцетом, а также применения стероловых форм витамина Д.
Оценка эффективности и безопасности препарата Парсабив также проводилась в 6-месячном рандомизированном цинакальцет-контролируемом двойном слепом исследовании с участием 683 пациентов с вторичными ГПТ и ХПН . находившихся на гемодиализе. Парсабив не уступал цинакальцету по доле пациентов, у которых происходило снижение средней концентрации ПТГ > 30% относительно исходного значения в течение периода оценки эффективности. Парсабив также превосходил цинакальцет в отношении вторичной конечной точки: среди пациентов, распределенных путем рандомизации в группу применения препарата Парсабив, доля пациентов, у которых произошло снижение средней концентрации ПТГ > 50% за время периода оценки эффективности, была выше, чем в группе применения цинакальцета. Статистически значимые различия между двумя группами отсутствовали в отношении вторичной конечной точки, которая оценивала среднее количество дней в неделю с эпизодами рвоты или тошноты на протяжении первых 8 недель лечения.
Оценка изменений концентрации альбумин-корригированного кальция в сыворотке крови крови при переводе пациентов с цинакальцета на препарат Парсабив проводилась у 147 пациентов. Результаты показали, что лечение препаратом Парсабив в начальной дозе 5 мг безопасно начинать через 7 дней после отмены цинакальцета при концентрации альбумин-корригированного кальция в сыворотке крови > 8,3 мг/дл на момент перевода.
Фармакокинетика
Всасывание
У пациентов с ХПН и вторичным ГПТ, которым требуется проведение гемодиализа, фармакокинетика этелкальцетида характеризовалась линейностью и не изменялась с течением времени как после в/в введения одной дозы (5 — 60 мг), так и после в/в введения повторных доз (2,5 — 20 мг). После в/в введения кинетика этелкальцетида демонстрировала триэкспоненциальный спад. На фоне в/в введения 3 раза в неделю в конце 3-4 ч процедуры гемодиализа концентрации этелкальцетида в плазме крови достигали практически равновесного состояния у пациентов с ХПН спустя 4 недели после начала лечения, при этом наблюдаемая кумуляция увеличивалась в 2-3 раза, а эффективный период полувыведения составлял 3-5 дней. У пациентов с нормальной функцией почек происходит быстрое выведение этелкальцетида, в то время как у пациентов с ХПН, которым требуется проведение гемодиализа, гемодиализ становится основным путем элиминации препарата.
Распределение
В популяционной фармакокинетической модели объем распределения в равновесном состоянии (Vss) составлял приблизительно 796 л. Этелкальцетид преимущественно связывается с альбумином сыворотки крови посредством обратимого ковалентного связывания. Способность к нековалентному связыванию у этелкальцетида низкая, а коэффициент несвязанной фракции составляет 0,53. Соотношение между концентрациями [|4С]-этелкальцетида в крови и в плазме крови составляет примерно 0,6.
Метаболизм
Этелкальцетид не метаболизируется изоферментами системы цитохромов CYP450. В крови этелкальцетид подвергается биотрансформации посредством обратимого дисульфидного обмена с эндогенными тиолами с преимущественным образованием конъюгатов с сывороточным альбумином.
Экспозиция продуктов биотрансформации в плазме крови была приблизительно в 5 раз выше, чем экспозиция этелкальцетида, а профиль концентрация-время продуктов биотрансформации был сопоставим с профилем этелкальцетида.
Выведение
У пациентов с ХПН, которым требовалось проведение гемодиализа, гемодиализ становился основным путем элиминации этелкальцетида. Эффективное выведение этелкальцетида происходило при клиренсе гемодиализа 7,66 л/ч. После введения одной дозы этелкальцетида, меченного радиоактивным изотопом, пациентам с ХПН и вторичным ГПТ, которым требовалось проведение гемодиализа, в диализате обнаружено примерно 60% [|4С]-этелкальцетида, а суммарно в моче и кале — 7% в течение 175 дней периода сбора.
Фармакокинетика у особых групп пациентов
Печеночная недостаточность
Формальные фармакокинетические исследования по применению этелкальцетида у пациентов с печеночной недостаточностью не проводились. Исследования in vitro показали, что этелкальцетид не является субстратом, ингибитором или индуктором ферментов CYP450.
Почечная недостаточность
Формальные фармакокинетические исследования по применению этелкальцетида у пациентов с почечной недостаточностью от легкой до тяжелой степени тяжести не проводились. Характеристика фармакокинетики этелкальцетида была составлена по пациентам с ХПН, находящимся на гемодиализе. Этелкальцетид предназначен для использования у пациентов с ХПН, находящихся на гемодиализе.
Масса тела, пол, расовая принадлежность и возраст
Результаты популяционного фармакокинетического анализа указывают на то, что масса тела (от 29 до 163 кг), пол, раса и возраст (от 20 до 93 лет) не оказывают влияния на фармакокинетику этелкальцетида.
Пациенты пожилого возраста
Фармакокинетика этелкальцетида у пациентов в возрасте 65 лет и старше аналогична таковой у пациентов младше 65 лет.
Пациенты детского возраста
Среди пациентов до 18 лет изучение фармакокинетики этелкальцетида не проводилось.
ПОКАЗАНИЯ
• лечение вторичного ГПТ у пациентов с XIIII, находящихся на гемодиализе.
ПРОТИВОПОКАЗАНИЯ
Гипокальциемия
Не следует начинать лечение препаратом Парсабив при концентрации альбумин-корригированного кальция в сыворотке крови ниже нижнего предела нормальных значений (см. раздел «Особые указания»).
Гиперчувствительность
Парсабив противопоказан пациентам с установленной гиперчувствительностью к действующему веществу или любому из вспомогательных веществ.
Беременность и период грудного вскармливания.
Детский возраст до 18 лет.
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И В ПЕРИОД ГРУДНОГО ВСКАРМЛИВАНИЯ
Беременность
Контролируемых исследований этелкальцетида с участием беременных женщин не проводилось. В доклинических исследованиях не отмечено какого-либо влияния на эмбриофетальное развитие у крыс и кроликов при внутривенном введении этелкальцетида в период органогенеза при экспозиции в 1.8-4.3 раза превышающей экспозицию, достигнутую у пациентов, получавших этелкальцетид при его введении в дозе 15 мг 3 раза в неделю. При более высокой экспозиции (в 2.7 — 7 раз выше, чем экспозиция у пациентов) отмечалось замедление роста плода, которое ассоциировалось с такими токсическими проявлениями у матери, как гипокальциемия, тремор, снижение массы тела и потребления пищи. В исследованиях на крысах в период пренатального и постнатального развития влияния на половое созревание, нейроповеденческую и репродуктивную функции в потомстве выявлено не было при экспозиции в 1,8 раз выше, чем у пациентов, получавших этелкальцетид в дозе 15 мг 3 раза в неделю. При экспозиции, схожей с таковой у пациентов, наблюдалось минимальное увеличение летальности потомства, задержка сроков родоразрешения и временное снижение скорости постнатального роста, что ассоциировалось с такими токсическими проявлениями у матери, как гипокальциемия, тремор, снижение массы тела и потребления пищи. Исследования на животных не всегда позволяют прогнозировать реакцию на препарат у человека. Поэтому неизвестно, может ли этелкальцетид оказывать негативное воздействие на плод при его назначении в период беременности, а значит применение препарата Парсабив во время беременности противопоказано.
Грудное вскармливание
Не известно, проникает ли этелкальцетид в грудное молоко. Исследования на крысах показали, [|4С]-этелкальцетид экскретируется в молоко в концентрациях, аналогичных таковым в плазме крови. Многие лекарственные средства проникают в грудное молоко у человека, поэтому, учитывая нежелательные реакции, которые может вызвать этелкальцетид у новорожденных, следует принять решение об отмене препарата Парсабив или прекращении грудного вскармливания, оценив предполагаемую пользу продолжения терапии препаратом Парсабив для матери и возможный риск негативного влияния на новорожденного.
Репродуктивная функция
Отсутствуют данные о влиянии препарата Парсабив на репродуктивную функцию человека. У крыс влияние на репродуктивную функцию не наблюдалось.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗЫ
Рекомендуемая начальная доза препарата Парсабив у взрослых составляет 5 мг в виде болюсного введения 3 раза в неделю.
Препарат Парсабив вводят через венозный катетер диализной системы в период промывки в конце процедуры гемодиализа, либо внутривенно после промывки катетера. Перед введением первой дозы препарата Парсабив, увеличением дозы препарата Парсабив или повторного назначения препарата Парсабив после временного прекращения лечения концентрация альбумин-корригированного кальция в сыворотке крови должна составлять > 8,3 мг/дл.
Дозу следует подбирать индивидуально в диапазоне от 2,5 до 15 мг. Препарат Парсабив не следует вводить чаще, чем 3 раза в неделю. Измерение концентрации ПТГ следует проводить через 4 недели после начала применения препарата Парсабив или изменения дозы, чтобы определить необходимость дополнительной коррекции дозы. Для достижения целевой концентрации ПТГ дозу препарата Парсабив можно увеличивать до максимальной дозы 15 мг 3 раза в неделю с шагом 2,5 или 5 мг, но не чаще чем каждые 4 недели. В случае снижения концентрации ПТГ ниже целевых значений дозу препарата Парсабив следует уменьшить или временно прекратить его применение. Для достижения целевых концентраций ПТГ после временного прекращения применения препарата Парсабив лечение следует возобновлять с использованием более низких доз.
Измерение концентрации кальция в сыворотке крови следует проводить в течение 1 недели после начала применения препарата Парсабив или изменения дозы. После определения поддерживающей дозы измерение альбумин-корри тированного кальция в сыворотке крови следует производить приблизительно каждые 4 недели. В случае клинически значимого снижения концентрации альбумин-корригированного кальция в сыворотке крови ниже 8,3 мг/дл и/или появления симптомов гипокальциемии, рекомендуется следующая тактика ведения:


В случае пропуска запланированной процедуры гемодиализа введение препарата Парсабив следует осуществить во время следующей процедуры в аналогичной дозе. Не следует вводить пропущенную дозу. Если введение препарата Парсабив было пропущено более 2 недель, то терапию следует возобновлять с дозы 5 мг (или 2,5 мг, если таковой была последняя введенная доза) и титровать дозу до достижения целевой концентрации ПТГ.
Препарат Парсабив можно применять отдельно или в сочетании со стероловыми формами витамина Д и/или фосфат-связующими препаратами.
Перевод с цинакальцета на препарат Парсабив
Терапию препаратом Парсабив не следует начинать раньше, чем через 7 дней после приема последней дозы цинакальцета и при концентрации альбумин-корригированного кальция > 8,3 мг/дл.
ПОБОЧНОЕ ДЕЙСТВИЕ
Рeзюме профиля безопасности
Принимая во внимание данные о применении препарата Парсабив у пациентов в плацебо-контролируемых исследованиях и в исследовании с активным контролем, наиболее распространенными нежелательными реакциями на фоне лечения препаратом Парсабив являются снижение концентрации кальция в крови, мышечные спазмы, диарею, тошноту и рвоту. У большинства пациентов эти явления были легкой или умеренной степени тяжести и носили временный характер. Прекращение лечения, обусловленное нежелательными реакциями, происходило преимущественно в связи со снижением концентрации кальция в крови, тошнотой и рвотой.
Перечень нежелательных реакций в таблицах
Нежелательные реакции, которые были определены как, по меньшей мере, возможно связанные с лечением этелкальцетидом на основании доказательных данных и оценки причинно-следственной связи, перечислены ниже согласно следующей классификации: очень часто (> 1/10); часто (> 1/100 до < 1/10); нечасто (> 1/1,000 до < 1/100); редко (> 1/10,000 до < 1/1,000); очень редко (< 1/10,000).
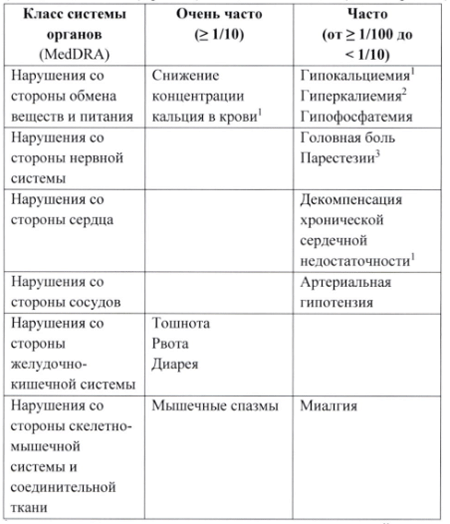
1 см. раздел «Описание отдельных нежелательных реакций».
2 Термин «гиперкалиемия» включал такие предпочтительные термины, как гиперкалиемия и увеличение концентрации калия в крови.
3 Термин «парестезии» включал такие предпочтительные термины, как парестезия и гипестезия.
Описание отдельных нежелательных реакций
Гипокальциемия
В программе клинических исследований препарата Парсабив бессимптомное снижение концентрации кальция ниже 7.5 мг/дл или бессимптомное снижение концентрации альбумин-корригированного кальция в диапазоне от 7,5 до 8,3 мг/дл, которое требовало лечения или которое исследователь определял как клинически значимое, регистрировалось как «снижение концентрации кальция в крови». Снижение концентрации альбумин-корригированного кальция ниже 8,3 мг/дл, сопровождающееся клиническими проявлениями, регистрировалось как «гипокальциемия» с указанием соответствующих объективных и субъективных симптомов. Большинство событий, представленных бессимптомным снижением концентрации кальция в крови и гипокальциемией с клиническими проявлениями, были легкой или умеренной степени тяжести. В объединенных данных плацебо-контролируемых исследований в группе лечения препаратом Парсабив по сравнению с группой плацебо была выше доля пациентов, у которых, по меньшей мере, однократно регистрировалась концентрация альбумин-корригированного кальция в сыворотке крови < 7,0 мг/дл (7,6% — в группе лечения; 3,1% — в группе плацебо). < 7,5 мг/дл (27,1% — в группе лечения; 5,5% — в группе плацебо) и < 8,3 мг/дл (78,6% — в группе лечения; 19,4% — в группе плацебо). В этих исследованиях 1% пациентов в группе лечения препаратом Парсабив и 0% пациентов группе плацебо прекратили лечение из-за нежелательного явления «низкая концентрация кальция в сыворотке крови».
Удлинение интервала QTc, обусловленное гипокальциемией
В объединенных данных плацебо-контролируемых исследований в группе лечения препаратом Парсабив по сравнению с группой плацебо была выше доля пациентов с максимальным удлинением интервала QTcF более 60 мсек относительно исходного уровня (1,2% — в группе лечения препаратом Парсабив, 0% — в группе плацебо). Доля пациентов, у которых после исходного обследования было зарегистрировано максимальное значение QTcF > 500 мсек (измерение проводилось перед процедурой диализа), составила в группе лечения 4,8%, а в группе плацебо — 1,9%.
Декомпенсация хронической сердечной недостаточности
В совокупности плацебо-контролируемых исследований доля пациентов, у которых наблюдалась декомпенсация хронической сердечной недостаточности, потребовавшее госпитализации, составила 2,2% в группе лечения препаратом Парсабив и 1,2% в группе плацебо.
ПЕРЕДОЗИРОВКА
Отсутствуют клинические данные о передозировке препарата Парсабив. Пациентам, получавшим диализ, препарат вводили в однократной дозе до 60 мг или в многократной дозе до 22,5 мг 3 раза в неделю в конце процедуры диализа. Передозировка препарата Парсабив может привести к гипокальциемии с клиническими проявлениями или без них и может потребовать лечения. Хотя Парсабив выводится при диализе, не проводилось изучение гемодиализа в качестве терапии передозировки препарата Парсабив. С целью своевременного проведения соответствующих вмешательств, при передозировке необходимо контролировать сывороточную концентрацию кальция и наблюдать пациента для выявления симптомов гипокальциемии (см. раздел «Способ применения и дозы»).
ВЗАИМОДЕЙСТВИЯ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ
Отсутствуют данные о фармакокинетических лекарственных взаимодействиях этелкальцетида. In vitro этелкальцетид не подавлял и не индуцировал активность изоферментов системы цитохромов CYP450, и не являлся их субстратом. In vitro этелкальцетид не являлся субстратом эффлюксных белков-транспортеров и белков-транспортеров захвата (Р-гликопротеина (Pgp), белка резистентности рака молочной железы (BCRP), транспортера органических анионов (ОАТ) 1 и 3, полипептида транспортера органических анионов (ОАТР) 1В1 и 1ВЗ, транспортера органических катионов (ОСТ) 2, транспортера пептидов (РЕРТ) 1 и 2). In vitro этелкальцетид также не демонстрировал способность ингибировать распространенные белки-транспортеры (Pgp, BCRP. ОАТ1, ОАТЗ, ОАТР1В1, ОАТР1ВЗ, ОСТ2 или экспортирующую помпу солей желчных кислот (ЭПЖК)).
Другие лекарственные средства, снижающие концентрацию кальция
Одновременное применение других лекарственных средств, снижающих концентрацию кальция в сыворотке крови, и препарата Парсабив может привести к повышению риска развития гипокальциемии (см. раздел «Особые указания»).
ОСОБЫЕ УКАЗАНИЯ
Гипокальциемия
Препарат Парсабив снижает сывороточную концентрацию кальция и может привести к развитию гипокальциемии (см. раздел «Побочное действие»). Лечение препаратом Парсабив не следует начинать у пациентов с ХПН, находящихся на гемодиализе, при концентрации альбумин-корригированного кальция в сыворотке крови ниже нижнего предела нормальных значений (см. раздел «Противопоказания»).
Следует наблюдать за пациентом для выявления гипокальциемии. Контроль концентрации кальция в сыворотке крови следует осуществлять перед началом терапии, в течение одной недели после начала терапии или коррекции дозы, а также каждые 4 недели лечения препаратом Парсабив (см. раздел «Способ применения и дозы»). Возможные клинические проявления гипокальциемии включают парестезии, миалгии, мышечные спазмы и судороги. Пациенту следует рекомендовать обратиться к врачу в случае появления симптомов гипокальциемии. При клинически значимом снижении концентрации альбумин-корригированного кальция в сыворотке крови необходимо провести мероприятия, направленные на повышение концентрации кальция в сыворотке крови (см. раздел «Способ применения и дозы»).
Желудочковая аритмия и удлинение интервала QT, обусловленное гипокальциемией
Снижение концентрации кальция в сыворотке крови может привести к удлинению интервала QT, что, в свою очередь, может сопровождаться развитием желудочковой аритмии. У пациентов с врожденным синдромом удлинения интервала QT, удлинением интервала QT в анамнезе, удлинением интервала QT или внезапной сердечной смертью в семейном анамнезе, а также другими состояниями-предикторами удлинения интервала QT и развития желудочковой аритмии необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения препаратом Парсабив.
Судороги
Порог судорожной готовности может быть снижен при значительном уменьшении концентрации кальция в сыворотке крови. У пациентов с судорожными расстройствами в анамнезе необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения препаратом Парсабив.
Декомпенсация хронической сердечной недостаточности
Снижение функции миокарда, гипотензия и хроническая сердечная недостаточность могут быть связаны со значительным уменьшением концентрации кальция в сыворотке крови. У пациентов с хронической сердечной недостаточностью в анамнезе (которая может ассоциироваться с уменьшением концентрации кальция в сыворотке крови) необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения препаратом Парсабив.
Одновременное применение с другими лекарственными средствами
Пациентам, получающим препарат Парсабив, не следует назначать цинакальцет (см. раздел «Способ применения и дозы»). Их одновременное применение может привести к развитию тяжелой гипокальциемии.
Препарат Парсабив следует с осторожностью назначать пациентам, получающим любые другие лекарственные средства, снижающие концентрацию кальция в сыворотке крови. Пациентам, получающим другие лекарственные средства, которые снижают концентрацию кальция в сыворотке крови, следует обеспечить тщательный контроль этого показателя.
Адинамическая болезнь кости
При длительном подавлении концентрации ПТГ ниже 100пг/мл возможно развитие адинамической болезни кости. При снижении концентрации ПТГ ниже рекомендуемого целевого диапазона необходимо уменьшить дозы или отменить терапию стероловыми формами витамина Д и/или препаратом Парсабив. После отмены терапию возобновляют в более низких дозах для поддержания концентрации ПТГ в пределах диапазона целевых значений (см. раздел «Способ применения и дозы»).
Особые группы пациентов
Дети
У детей безопасность и эффективность препарата Парсабив не установлена.
Пожилые пациенты
Отсутствовали клинически значимые различия безопасности и эффективности между пациентами в возрасте 65 лет и старше и пациентами более молодого возраста (> 18 и <65 лет). Не были обнаружены различия концентрации этелкальцетида в плазме крови между пациентами в возрасте 65 лет и старше и пациентами более молодого возраста (> 18 и < 65 лет). Из 503 пациентов, получавших препарат Парсабив в плацебо-контролируемых исследованиях, 177 пациентов (35,2%) были в возрасте 65 лет и старше.
Печеночная недостаточность
Этелкальцетид не подвергается печеночному метаболизму; поэтому ожидается, что печеночная недостаточность не будет оказывать значительного эффекта на выведение этелкальцетида. Влияние печеночной недостаточности на фармакокинетику этелкальцетид не изучалось (см. раздел «Фармакокинетика»).
Почечная недостаточность
Парсабив показан пациентам, находящимся на гемодиализе. Влияние степени тяжести почечной недостаточности на фармакокинетику препарата Парсабив не изучено (см. раздел «Фармакокинетика»).
Иммуногенностъ
Оценка иммуногенности этелкальцетида проводилась с помощью иммунологического исследования на основе поверхностного плазмонного резонанса, которое позволяло обнаружить связывающие антитела к этелкальцетиду. В клинических исследованиях у 7.1% (71 из 995) пациентов с вторичным гиперпаратиреозом (ГПТ), получавших лечение этелкальцетидом в период до 6 месяцев, обнаруживались связывающие антитела (при этом у 80,3% из них [у 57 из 71] антитела были выявлены при исходном обследовании).
Не отмечено изменения фармакокинетического профиля, клинического ответа или профиля безопасности, вызванных наличием антител к этелкальцетиду, изначально присутствовавших, или выработанных во время лечения. При подозрении на образование антител к этелкальцетиду, которое сопровождается клинически значимыми эффектами, пожалуйста, свяжитесь с компанией «Амджен» для решения вопроса о проведении лабораторного исследования для выявления антител.
Особые указания по применению и меры предосторожности
Препарат Парсабив не требует смешивания или разведения перед применением. Раствор является прозрачным и бесцветным. Перед применением препаратов для парентерального введения необходимо предварительно произвести визуальный осмотр для выявления инородных частиц и изменения цвета. Раствор нельзя применять при помутнении или изменении цвета, содержании мутных или окрашенных включений.
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ ТРАНСПОРТНЫМИ СРЕДСТВАМИ И МЕХАНИЗМАМИ
Исследования влияния препарата Парсабив на способность управлять транспортными средствами и механизмами не проводились.
ФОРМА ВЫПУСКА
Раствор для внутривенного введения 2,5 мг/ 0,5 мл, 5,0 мг/1 мл, 10 мг/ 2 мл.
По 0,5 мл, 1,0 мл или 2,0 мл раствора во флаконе объемом 3 мл из стекла гидролитического класса с эластомерной пробкой, ламинированной фторполимером, алюминиевым колпачком и отламывающимся полипропиленовым колпачком.
6 флаконов помещают в пачку картонную вместе с инструкцией по применению. На каждую пачку наклеивают защитные этикетки — контроль первого вскрытия, имеющие продольную цветную полосу.
УСЛОВИЯ ХРАНЕНИЯ
Хранить при температуре от 2°С до 8°С. Не замораживать.
Хранить в оригинальной упаковке для защиты от света.
Не встряхивать.
Хранить в недоступном для детей месте!
При изъятии из холодильной камеры возможно хранение лекарственного препарата при температуре не выше 25°С в течение 7 дней в оригинальной упаковке (картонной пачке), в случае хранения флакона без картонной пачки — в течение 4 часов, избегая воздействия прямых солнечных лучей.
СРОК годности
2 года.
Не применять по истечении срока годности, указанного на упаковке.
УСЛОВИЯ ОТПУСКА
Отпускают по рецепту.
ЮРИДИЧЕСКОЕ ЛИЦО, НА ИМЯ КОТОРОГО ВЫДАНО РЕГИСТРАЦИОННОЕ УДОСТОВЕРЕНИЕ
«Амджен Европа Б.В.» Минервум 7061 4817 ZK Бреда Нидерланды
ПРОИЗОДИТЕЛЬ, ОСУЩЕСТВЛЯЮЩИЙ выпускающий контроль КАЧЕСТВА
«Амджен Европа Б.В.» Минервум 7061 4817 ZK Бреда Нидерланды
ПРЕДСТАВИТЕЛЬ В РОССИЙСКОЙ ФЕДЕРАЦИИ
ООО «Амджен»
123317, Москва, Пресненская наб., дом 8, корпус 1; 7-й этаж
Купить Парсабив в megapteka.ru
*Цены в Москве. Точная цена в Вашем городе будет указана на сайте аптеки.
Комментарии
(видны только специалистам, верифицированным редакцией МЕДИ РУ)
|
|
Условия хранения
В оригинальной упаковке для защиты от света, при температуре 2-8 град. (не замораживать)
Взаимодействие с другими препаратами
Одновременное применение других лекарственных средств, снижающих концентрацию кальция в сыворотке крови, и этелкальцетида может привести к повышению риска развития гипокальциемии.
Побочные действия
Со стороны обмена веществ: очень часто — снижение концентрации кальция в крови; часто — гипокальциемия, гиперкалиемия, гипофосфатемия.
Со стороны нервной системы: часто — головная боль, парестезии.
Со стороны сердечно-сосудистой системы: часто — декомпенсация хронической сердечной недостаточности, артериальная гипотензия.
Со стороны пищеварительной системы: очень часто — тошнота, рвота, диарея.
Со стороны костно-мышечной системы: очень часто — мышечные спазмы; часто — миалгия.
Способ применения и дозы
Вводят болюсно 3 раза в неделю.
Введение проводят через венозный катетер диализной системы в период промывки в конце процедуры гемодиализа, либо внутривенно после промывки катетера.
Перед введением первой дозы этелкальцида, увеличением дозы или повторного применения после временного прекращения лечения концентрация альбумин-корригированного кальция в сыворотке крови должна составлять ≥8.3 мг/дл.
Рекомендуемая начальная доза — 5 мг.
Дозу следует подбирать индивидуально в диапазоне от 2.5 до 15 мг.
В случае клинически значимого снижения концентрации альбумин-корригированного кальция в сыворотке крови ниже 8.3 мг/дл и/или появления симптомов гипокальциемии проводится коррекция лечения по специальной схеме.
Препарат противопоказан для применения у детей и подростков в возрасте до 18 лет
Противопоказания
Гипокальциемия (концентрация альбумин-корригированного кальция в сыворотке крови ниже нижнего предела нормальных значений), беременность, период грудного вскармливания, возраст до 18 лет, повышенная чувствительность к этелкальцетиду.
С осторожностью (меры предосторожности)
Препарат разрешен для применения при нарушении функции печени
Предназначен для применения у пациентов, находящихся на гемодиализе.
Особые указания
Этелкальцетид снижает сывороточную концентрацию кальция и может привести к развитию гипокальциемии.
Следует наблюдать за пациентом для выявления гипокальциемии. Контроль концентрации кальция в сыворотке крови следует осуществлять перед началом терапии, в течение одной недели после начала терапии или коррекции дозы, а также каждые 4 недели лечения этелкальцетидом. Возможные клинические проявления гипокальциемии включают парестезии, миалгии, мышечные спазмы и судороги. Пациенту следует рекомендовать обратиться к врачу в случае появления симптомов гипокальциемии. При клинически значимом снижении концентрации альбумин-корригированного кальция в сыворотке крови необходимо провести мероприятия, направленные на повышение концентрации кальция в сыворотке.
Снижение концентрации кальция в сыворотке крови может привести к удлинению интервала QT, что, в свою очередь, может сопровождаться развитием желудочковой аритмии. У пациентов с врожденным синдромом удлинения интервала QT, удлинением интервала QT в анамнезе, удлинением интервала QT или внезапной сердечной смертью в семейном анамнезе, а также другими состояниями-предикторами удлинения интервала QTи развития желудочковой аритмии необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения.
Порог судорожной готовности может быть снижен при значительном уменьшении концентрации кальция в сыворотке крови. У пациентов с судорожными расстройствами в анамнезе необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения.
Снижение функции миокарда, артериальная гипотензия и хроническая сердечная недостаточность могут быть связаны со значительным уменьшением концентрации кальция в сыворотке крови. У пациентов с хронической сердечной недостаточностью в анамнезе (которая может ассоциироваться с уменьшением концентрации кальция в сыворотке крови) необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения.
Пациентам, получающим этелкальцетид не следует назначать цинакальцет. Их одновременное применение может привести к развитию тяжелой гипокальциемии.
С осторожностью применять у пациентов, получающих любые другие лекарственные средства, снижающие концентрацию кальция в сыворотке крови. В таких случаях необходимо тщательно контролировать концентрацию кальция в крови.
При длительном подавлении концентрации ПТГ ниже 100 пг/мл возможно развитие адинамической болезни кости. При снижении концентрации ПТГ ниже рекомендуемого целевого диапазона необходимо уменьшить дозы или отменить терапию стероловыми формами витамина D и/или этелкальцетидом. После отмены терапию возобновляют в более низких дозах для поддержания концентрации ПТГ’ в пределах диапазона целевых значений.
Не отмечено изменения фармакокинетического профиля, клинического ответа или профиля безопасности, вызванных наличием антител к этелкальцетиду, изначально присутствовавших, или выработанных во время лечения.
Применение при беременности и кормлении грудью
Противопоказано применение при беременности и в период грудного вскармливания.
Показания к применению
Лечение вторичного гиперпаратиреоза у пациентов с хронической почечной недостаточностью, находящихся на гемодиализе.
Фармакокинетика
У пациентов с хронической почечной недостаточностью и вторичным гиперпаратиреозом, которым требуется проведение гемодиализа, фармакокинетика этелкальцетида характеризовалась линейностью и не изменялась с течением времени как после в/в введения однократной дозы (5-60 мг), так и после в/в введения повторных доз (2.5-20 мг). После в/в введения кинетика этелкальцетида демонстрировала триэкспоненциальный спад. На фоне в/в введения 3 раза в неделю в конце 3-4 ч процедуры гемодиализа концентрации этелкальцетида в плазме крови достигали практически равновесного состояния у пациентов с ХПН спустя 4 недели после начала лечения, при этом наблюдаемая кумуляция увеличивалась в 2-3 раза, а эффективный период полувыведения составлял 3-5 дней. У пациентов с нормальной функцией почек происходит быстрое выведение этелкальцетида, в то время как у пациентов с ХПН. которым требуется проведение гемодиализа, гемодиализ становится основным путем элиминации препарата.
В популяционной фармакокинетической модели Vss составлял приблизительно 796 л. Этелкальцетид преимущественно связывается с альбумином сыворотки крови посредством обратимого ковалентного связывания. Способность к нековалентному связыванию у этелкальцетида низкая, а коэффициент несвязанной фракции составляет 0.53. Соотношение между концентрациями [14С]-этелкальцетида в крови и в плазме крови составляет примерно 0.6.
В крови этелкальцетид подвергается биотрансформации посредством обратимого дисульфидного обмена с эндогенными тиолами с преимущественным образованием конъюгатов с сывороточным альбумином.
Экспозиция продуктов биотрансформации в плазме крови была приблизительно в 5 раз выше, чем экспозиция этелкальцетида, а профиль концентрация-время продуктов биотрансформации был сопоставим с профилем этелкальцетида.
У пациентов с хронической почечной недостаточностью, которым требовалось проведение гемодиализа, гемодиализ становился основным путем элиминации этелкальцетида. Эффективное выведение этелкальцетида происходило при клиренсе гемодиализа 7.66 л/ч. После введения одной дозы этелкальцетида, меченного радиоактивным изотопом, пациентам с ХПН и вторичным ГПТ, которым требовалось проведение гемодиализа, в диализате обнаружено примерно 60% [14С]-этелкальцетида, а суммарно в моче и кале — 7% в течение 175 дней периода сбора.
Фармакодинамика
Антипаратиреоидное средство, кальцимиметик, синтетический пептид. Этелкальцетид специфически связывается с кальций-чувствительными рецепторами (CaSR) и вызывает их активацию, что приводит к снижению секреции паратиреоидного гормона (ПТГ) главными клетками паращитовидной железы.
У пациентов, находящихся на гемодиализе, снижение концентрации ПТГ коррелирует с концентрацией этелкальцетида в плазме крови. Уменьшение концентрации ПТГ ассоциируется с сопутствующим снижением концентраций кальция и фосфатов в сыворотке крови.
После однократного в/в болюсного введения этелкальцетида происходит быстрое (в течение 30 мин) снижение концентрации ПТГ. Выраженность и продолжительность снижения ПТГ усиливаются с увеличением дозы. Снижение концентрации ПТГ ведет к снижению концентрации кальция и ограничивает увеличение концентрации фосфатов после диализа. При в/в болюсном введении этелкальцетида 3 раза в неделю снижение концентрации ПТГ сохранялось в течение 6 месяцев.
Срок годности от даты изготовления
4 года.
Для покупок в нашей интернет-аптеке выберите требуемый товар и добавьте его в корзину. Далее перейдите в Корзину и нажмите на кнопку «Перейти к оформлению».
Оформление заказа выглядит следующим образом:
- Заполните полностью форму по последовательным этапам: данные о себе, способ и адрес доставки*, способ оплаты;
- При оформлении доставки по адресу рекомендуем в комментарии к заказу написать информацию, которая поможет курьеру вас найти;
- Нажмите на кнопку «Оформить заказ».
Интернет-заказы принимаются круглосуточно. Обработка заказов производится согласно графику работы аптек в г. Краснодаре.
*Важно: Курьерская доставка лекарственных препаратов, отпускаемых по рецепту, наркотических и психотропных лекарственных препаратов, а также спиртосодержащих лекарственных препаратов с объёмной долей этилового спирта свыше 25% не осуществляется в соответствии с
Постановлением Правительства РФ №697 от 16.05.2020. Доставка курьером доступна в интернет-аптеке «Фармсервис» только для не рецептурных лекарственных средств и изделий медицинского назначения. Для остальных категории товаров вы можете выбрать самовывоз из наших аптек г. Краснодаре.
Подробная информация о правилах розничной продажи интернет-аптекой «Фармсервис» лекарственных препаратов для медицинского применения дистанционным способом приведена в разделе «Правила дистанционной торговли».
В интернет-аптеке «Фармсервис» доступны следующие способы оплаты:
- Наличные денежные средства и банковская карты при получении — при самовывозе из аптеки в г. Краснодаре либо при доставке курьерской службой вы оплачиваете заказ наличными или банковской картой (МИР, Visa, MasterCard) в момент получения, получаете товар и кассовый чек. При получении заказа в курьерской службе от вас дополнительно потребуется подпись товаросопроводительных документов;
- Банковская карта (МИР, Visa, MasterCard) при оформлении заказа в интернет-аптеке — в этом случае на странице оплаты банка-партнёра потребуется ввести номер карты, срок действия и CVC-код. При необходимости банк попросит вас ввести смс-код для подтверждения платежа. После оплаты вы получите электронный кассовый чек от оператора фискальных данных. Для получения заказа в аптеке либо при курьерской доставке вам потребуется назвать номер заказа и предъявить документ, удостоверяющий вашу личность — паспорт гражданина РФ/СССР, заграничный паспорт, военный билет или удостоверение личности военнослужащего РФ.
Важно:
- Водительское удостоверение, студенческий билет, ИНН и т.д. не являются документами, удостоверяющими личность на территории Российской Федерации;
- Оплата заказа в момент оформления доступна исключительно для товара, разрешённого к торговле дистанционным способом. Все прочие категории товара Вы можете оплатить в наших аптеках г. Краснодара при получении заказа. Для рецептурных лекарственных средств дополнительно потребуется рецепт, выписанный соответствующей медицинской организацией.
Подробная информация о правилах розничной продажи интернет-аптекой «Фармсервис» лекарственных препаратов для медицинского применения дистанционным способом приведена в разделе «Правила дистанционной торговли».
В интернет-аптеке доступны следующие способы доставки:
Самовывоз из аптек г. Краснодара
Вы можете самостоятельно забрать заказ в одной из аптек г. Краснодара — при оформлении заказа выберите способ доставки «Самовывоз» и аптеку, из которой хотели бы забрать заказ. Для получения заказа дождитесь уведомление на электронную почту о готовности заказа и сообщите провизору в аптеке его номер. В случае оплаты заказа при оформлении на сайте для получения товара потребуется предъявить документ, удостоверяющий вашу личность — паспорт гражданина РФ/СССР, заграничный паспорт, военный билет или удостоверение личности военнослужащего РФ.
При фактическом наличии товаров в аптеке сборка вашего заказа составит не более 1 часа. При наличии в заказе товаров под заказ время сборки будет увеличено на время заказа и доставки отсутствующих товаров в выбранную вами аптеку для самовывоза.
При оформлении самовывоза из аптеки без оплаты заказа товары будут забронированы за вами в течение 72 часов. По истечении этого срока заказ будет отменён. При необходимости продления срока бронирования позвоните в выбранную вами аптеку самовывоза и сообщите об этом провизору.
Доставка
Заказы, оформленные до 14:00, будут доставлены вам на следующий рабочий день.
Заказы, оформленные после 14:00, будут доставлены вам через рабочий день.
Сроки доставки в регионы Российской Федерации определяются автоматически на основании графика доставок курьерской службы. Среднее время доставки заказов составляет 4-6 рабочих дней.
Стоимость доставки зависит от веса и габаритов заказанного вами товара и рассчитывается по тарифам курьерской службы.
Важно: при наличии в заказе товаров под заказ время доставки будет увеличено на время поставки в аптеку товара под заказ.
Общая информация
Устаревшее наименование
—
Владелец
Номер регистрационного удостоверения РФ
ЛП-№(003004)-(РГ-RU)
Действующее вещество (МНН)
Форма выпуска / дозировка
Раствор для внутривенного введения
Лекарственная форма ГРЛС
Раствор в/в
Состав
Препарат Парсабив содержит:
Действующим веществом является этелкальцетид.
Каждый флакон содержит 2,5 мг этелкальцетида в 0,5 мл раствора (5 мг/мл).
Прочими ингредиентами (вспомогательными веществами) являются натрия хлорид, янтарная кислота, хлористоводородная кислота, натрия гидроксид, вода для инъекций (см. раздел: препарат Парсабив содержит натрий).
Описание препарата
Прозрачная бесцветная жидкость, свободная от механических включений.
Фармако-терапевтическая группа
Средства, регулирующие обмен кальция; антипаратиреоидные средства, другие антипаратиреоидные средства
раствор для внутривенного введения
Один флакон 0,5 мл содержит:
Действующее вещество: 3.1 мг этелкальцетида гидрохлорида (2,5 мг в пересчете на этелкальцетид) в 0,5 мл раствора (5 мг/мл)
Вспомогательные вещества: натрия хлорид — 4,3 мг, янтарная кислота -0,6мг, хлористоводородная кислота — до рН 3,3, натрия гидроксид — до рН 3,3, вода для инъекций — до объема 0,5 мл
Один флакон 1,0 мл содержит
Действующее вещество:
6.2 мг этелкальцетида гидрохлорида (5 мг в пересчете на этелкальцетид) в 1 мл раствора (5 мг/мл)
Вспомогательные вещества: натрия хлорид — 8,5 мг, янтарная кислота — 1,2 мг, хлористоводородная кислота — до рН 3,3, натрия гидроксид — до рН 3,3, вода для инъекций — до объема 1,0 мл
Один флакон 2,0 мл содержит
Действующее вещество:
12,3 мг этелкальцетида гидрохлорида (10 мг в пересчете на этелкальцетид) в 2 мл раствора (5 мг/мл)
Вспомогательные вещества: натрия хлорид — 17,0 мг, янтарная кислота -2,4 мг, хлористоводородная кислота — до рН 3,3, натрия гидроксид — до рН 3,3, вода для инъекций — до объема 2,0 мл
Прозрачная бесцветная жидкость, свободная от механических включений.
Антипаратиреоидное средство
Код
ATX
Н05ВХ04
Фармакодинамика
Механизм действия
Этелкальцетид представляет собой синтетический пептид, кальцимиметик. Этелкальцетид специфически связывается с кальций-чувствительными рецепторами (CaSR) и вызывает их активацию, что приводит к снижению секреции паратиреоидного гормона (ПТГ) главными клетками паращитовидной железы. У пациентов, находящихся на гемодиализе, снижение концентрации ПТГ коррелирует с концентрацией этелкальцетида в плазме крови. Уменьшение концентрации ПТГ ассоциируется с сопутствующим снижением концентраций кальция и фосфатов в сыворотке крови.
После однократного внутривенного (в/в) болюсного введения этелкальцетида происходит быстрое (в течение 30 минут) снижение концентрации ПТГ. Выраженность и продолжительность снижения ПТГ усиливаются с увеличением дозы. Снижение концентрации ПТГ ведет к снижению концентрации кальция и ограничивает увеличение концентрации фосфатов после диализа. При в/в болюсном введении этелкальцетида 3 раза в неделю снижение концентрации ПТГ сохранялось в течение 6 месяцев.
Данные клинических исследований
Оценка препарата Парсабив проводилась в трех 6-месячных многоцентровых рандомизированных двойных-слепых контролируемых клинических исследованиях у пациентов с вторичным гиперпаратиреозом (ГПТ) при хронической почечной недостаточности (ХПН). находящихся на гемодиализе. Изучение препарата Парсабив также проводилось в рамках одного многоцентрового неконтролируемого исследования по оценке безопасности перевода пациентов с вторичным ГПТ, находившихся на гемодиализе, с перорального приема цинакальцета на в/в введение препарата Парсабив.
Эффективность и безопасность препарата Парсабив у пациентов с вторичным ГПТ с ХПН. находившихся на гемодиализе 3 раза в неделю, оценивались в двух 6-месячных многоцентровых рандомизированных двойных-слепых плацебо-контролируемых исследованиях. В каждом из исследований первичная конечная точка была представлена долей пациентов, достигших на протяжении периода оценки эффективности (ЕАР) снижения концентрации ПТГ более чем на 30% по сравнению с исходным значением. Вторичные конечные точки были представлены долей пациентов со средним уровнем ПТГ < 300 пг/мл во время периода оценки эффективности, процентным изменением относительно исходных уровней во время периода оценки эффективности таких показателей, как концентрация ПТГ. альбумин-корригированного кальция в сыворотке крови, произведения кальций-фосфор (Са х Р).
В данных плацебо-контролируемых исследованиях участвовали в общей сложности 1,023 пациентов (509 получали Парсабив, 514 — плацебо). Демографические и исходные характеристики обеих групп в обоих исследованиях были сопоставимы. В исследованиях были получены схожие результаты: на протяжении периода оценки эффективности препарата Парсабив в сравнении с плацебо статистически значимо увеличивал долю пациентов, у которых происходило снижение средней концентрации ПТГ более чем на 30% относительно исходного значения, увеличивал долю пациентов со средней концентрацией ПТГ < 300 пг/мл (вторичная оценка эффективности), а также вызывал статистически значимое снижение концентрации ПТГ, альбумин-корригированного кальция, фосфатов и произведения кальций-фосфор (Са х Р). Снижение концентрации ПТГ, альбумин-корригированного кальция, фосфатов и Са х Р в сыворотке крови поддерживалось на протяжении 78 недель лечения. Парсабив вызывал снижение концентрации ПТГ независимо от его исходного значения, продолжительности диализа, предшествующего лечения цинакальцетом, а также применения стероловых форм витамина Д.
Оценка эффективности и безопасности препарата Парсабив также проводилась в 6-месячном рандомизированном цинакальцет-контролируемом двойном слепом исследовании с участием 683 пациентов с вторичными ГПТ и ХПН . находившихся на гемодиализе. Парсабив не уступал цинакальцету по доле пациентов, у которых происходило снижение средней концентрации ПТГ > 30% относительно исходного значения в течение периода оценки эффективности. Парсабив также превосходил цинакальцет в отношении вторичной конечной точки: среди пациентов, распределенных путем рандомизации в группу применения препарата Парсабив, доля пациентов, у которых произошло снижение средней концентрации ПТГ > 50% за время периода оценки эффективности, была выше, чем в группе применения цинакальцета. Статистически значимые различия между двумя группами отсутствовали в отношении вторичной конечной точки, которая оценивала среднее количество дней в неделю с эпизодами рвоты или тошноты на протяжении первых 8 недель лечения.
Оценка изменений концентрации альбумин-корригированного кальция в сыворотке крови крови при переводе пациентов с цинакальцета на препарат Парсабив проводилась у 147 пациентов. Результаты показали, что лечение препаратом Парсабив в начальной дозе 5 мг безопасно начинать через 7 дней после отмены цинакальцета при концентрации альбумин-корригированного кальция в сыворотке крови > 8,3 мг/дл на момент перевода.
Фармакокинетика
Всасывание
У пациентов с ХПН и вторичным ГПТ, которым требуется проведение гемодиализа, фармакокинетика этелкальцетида характеризовалась линейностью и не изменялась с течением времени как после в/в введения одной дозы (5 — 60 мг), так и после в/в введения повторных доз (2,5 — 20 мг). После в/в введения кинетика этелкальцетида демонстрировала триэкспоненциальный спад. На фоне в/в введения 3 раза в неделю в конце 3-4 ч процедуры гемодиализа концентрации этелкальцетида в плазме крови достигали практически равновесного состояния у пациентов с ХПН спустя 4 недели после начала лечения, при этом наблюдаемая кумуляция увеличивалась в 2-3 раза, а эффективный период полувыведения составлял 3-5 дней. У пациентов с нормальной функцией почек происходит быстрое выведение этелкальцетида, в то время как у пациентов с ХПН, которым требуется проведение гемодиализа, гемодиализ становится основным путем элиминации препарата.
Распределение
В популяционной фармакокинетической модели объем распределения в равновесном состоянии (Vss) составлял приблизительно 796 л. Этелкальцетид преимущественно связывается с альбумином сыворотки крови посредством обратимого ковалентного связывания. Способность к нековалентному связыванию у этелкальцетида низкая, а коэффициент несвязанной фракции составляет 0,53. Соотношение между концентрациями [|4С]-этелкальцетида в крови и в плазме крови составляет примерно 0,6.
Метаболизм
Этелкальцетид не метаболизируется изоферментами системы цитохромов CYP450. В крови этелкальцетид подвергается биотрансформации посредством обратимого дисульфидного обмена с эндогенными тиолами с преимущественным образованием конъюгатов с сывороточным альбумином.
Экспозиция продуктов биотрансформации в плазме крови была приблизительно в 5 раз выше, чем экспозиция этелкальцетида, а профиль концентрация-время продуктов биотрансформации был сопоставим с профилем этелкальцетида.
Выведение
У пациентов с ХПН, которым требовалось проведение гемодиализа, гемодиализ становился основным путем элиминации этелкальцетида. Эффективное выведение этелкальцетида происходило при клиренсе гемодиализа 7,66 л/ч. После введения одной дозы этелкальцетида, меченного радиоактивным изотопом, пациентам с ХПН и вторичным ГПТ, которым требовалось проведение гемодиализа, в диализате обнаружено примерно 60% [|4С]-этелкальцетида, а суммарно в моче и кале — 7% в течение 175 дней периода сбора.
Фармакокинетика у особых групп пациентов
Печеночная недостаточность
Формальные фармакокинетические исследования по применению этелкальцетида у пациентов с печеночной недостаточностью не проводились. Исследования in vitro показали, что этелкальцетид не является субстратом, ингибитором или индуктором ферментов CYP450.
Почечная недостаточность
Формальные фармакокинетические исследования по применению этелкальцетида у пациентов с почечной недостаточностью от легкой до тяжелой степени тяжести не проводились. Характеристика фармакокинетики этелкальцетида была составлена по пациентам с ХПН, находящимся на гемодиализе. Этелкальцетид предназначен для использования у пациентов с ХПН, находящихся на гемодиализе.
Масса тела, пол, расовая принадлежность и возраст
Результаты популяционного фармакокинетического анализа указывают на то, что масса тела (от 29 до 163 кг), пол, раса и возраст (от 20 до 93 лет) не оказывают влияния на фармакокинетику этелкальцетида.
Пациенты пожилого возраста
Фармакокинетика этелкальцетида у пациентов в возрасте 65 лет и старше аналогична таковой у пациентов младше 65 лет.
Пациенты детского возраста
Среди пациентов до 18 лет изучение фармакокинетики этелкальцетида не проводилось.
• лечение вторичного ГПТ у пациентов с XIIII, находящихся на гемодиализе.
Гипокальциемия
Не следует начинать лечение препаратом Парсабив при концентрации альбумин-корригированного кальция в сыворотке крови ниже нижнего предела нормальных значений (см. раздел «Особые указания»).
Гиперчувствительность
Парсабив противопоказан пациентам с установленной гиперчувствительностью к действующему веществу или любому из вспомогательных веществ.
Беременность и период грудного вскармливания.
Детский возраст до
18
лет.
ПРИМЕНЕНИЕ ПРИ БЕРЕМЕННОСТИ И В ПЕРИОД ГРУДНОГО ВСКАРМЛИВАНИЯ
Беременность
Контролируемых исследований этелкальцетида с участием беременных женщин не проводилось. В доклинических исследованиях не отмечено какого-либо влияния на эмбриофетальное развитие у крыс и кроликов при внутривенном введении этелкальцетида в период органогенеза при экспозиции в 1.8-4.3 раза превышающей экспозицию, достигнутую у пациентов, получавших этелкальцетид при его введении в дозе 15 мг 3 раза в неделю. При более высокой экспозиции (в 2.7 — 7 раз выше, чем экспозиция у пациентов) отмечалось замедление роста плода, которое ассоциировалось с такими токсическими проявлениями у матери, как гипокальциемия, тремор, снижение массы тела и потребления пищи. В исследованиях на крысах в период пренатального и постнатального развития влияния на половое созревание, нейроповеденческую и репродуктивную функции в потомстве выявлено не было при экспозиции в 1,8 раз выше, чем у пациентов, получавших этелкальцетид в дозе 15 мг 3 раза в неделю. При экспозиции, схожей с таковой у пациентов, наблюдалось минимальное увеличение летальности потомства, задержка сроков родоразрешения и временное снижение скорости постнатального роста, что ассоциировалось с такими токсическими проявлениями у матери, как гипокальциемия, тремор, снижение массы тела и потребления пищи. Исследования на животных не всегда позволяют прогнозировать реакцию на препарат у человека. Поэтому неизвестно, может ли этелкальцетид оказывать негативное воздействие на плод при его назначении в период беременности, а значит применение препарата Парсабив во время беременности противопоказано.
Грудное вскармливание
Не известно, проникает ли этелкальцетид в грудное молоко. Исследования на крысах показали, [|4С]-этелкальцетид экскретируется в молоко в концентрациях, аналогичных таковым в плазме крови. Многие лекарственные средства проникают в грудное молоко у человека, поэтому, учитывая нежелательные реакции, которые может вызвать этелкальцетид у новорожденных, следует принять решение об отмене препарата Парсабив или прекращении грудного вскармливания, оценив предполагаемую пользу продолжения терапии препаратом Парсабив для матери и возможный риск негативного влияния на новорожденного.
Репродуктивная функция
Отсутствуют данные о влиянии препарата Парсабив на репродуктивную функцию человека. У крыс влияние на репродуктивную функцию не наблюдалось.
Способ применения и дозировка
Рекомендуемая начальная доза препарата Парсабив у взрослых составляет 5 мг в виде болюсного введения 3 раза в неделю.
Препарат Парсабив вводят через венозный катетер диализной системы в период промывки в конце процедуры гемодиализа, либо внутривенно после промывки катетера. Перед введением первой дозы препарата Парсабив, увеличением дозы препарата Парсабив или повторного назначения препарата Парсабив после временного прекращения лечения концентрация альбумин-корригированного кальция в сыворотке крови должна составлять > 8,3 мг/дл.
Дозу следует подбирать индивидуально в диапазоне от 2,5 до 15 мг. Препарат Парсабив не следует вводить чаще, чем 3 раза в неделю. Измерение концентрации ПТГ следует проводить через 4 недели после начала применения препарата Парсабив или изменения дозы, чтобы определить необходимость дополнительной коррекции дозы. Для достижения целевой концентрации ПТГ дозу препарата Парсабив можно увеличивать до максимальной дозы 15 мг 3 раза в неделю с шагом 2,5 или 5 мг, но не чаще чем каждые 4 недели. В случае снижения концентрации ПТГ ниже целевых значений дозу препарата Парсабив следует уменьшить или временно прекратить его применение. Для достижения целевых концентраций ПТГ после временного прекращения применения препарата Парсабив лечение следует возобновлять с использованием более низких доз.
Измерение концентрации кальция в сыворотке крови следует проводить в течение 1 недели после начала применения препарата Парсабив или изменения дозы. После определения поддерживающей дозы измерение альбумин-корри тированного кальция в сыворотке крови следует производить приблизительно каждые 4 недели. В случае клинически значимого снижения концентрации альбумин-корригированного кальция в сыворотке крови ниже 8,3 мг/дл и/или появления симптомов гипокальциемии, рекомендуется следующая тактика ведения:
В случае пропуска запланированной процедуры гемодиализа введение препарата Парсабив следует осуществить во время следующей процедуры в аналогичной дозе. Не следует вводить пропущенную дозу. Если введение препарата Парсабив было пропущено более 2 недель, то терапию следует возобновлять с дозы 5 мг (или 2,5 мг, если таковой была последняя введенная доза) и титровать дозу до достижения целевой концентрации ПТГ.
Препарат Парсабив можно применять отдельно или в сочетании со стероловыми формами витамина Д и/или фосфат-связующими препаратами.
Перевод с цинакальцета на препарат Парсабив
Терапию препаратом Парсабив не следует начинать раньше, чем через 7 дней после приема последней дозы цинакальцета и при концентрации альбумин-корригированного кальция > 8,3 мг/дл.
Рeзюме профиля безопасности
Принимая во внимание данные о применении препарата Парсабив у пациентов в плацебо-контролируемых исследованиях и в исследовании с активным контролем, наиболее распространенными нежелательными реакциями на фоне лечения препаратом Парсабив являются снижение концентрации кальция в крови, мышечные спазмы, диарею, тошноту и рвоту. У большинства пациентов эти явления были легкой или умеренной степени тяжести и носили временный характер. Прекращение лечения, обусловленное нежелательными реакциями, происходило преимущественно в связи со снижением концентрации кальция в крови, тошнотой и рвотой.
Перечень нежелательных реакций в таблицах
Нежелательные реакции, которые были определены как, по меньшей мере, возможно связанные с лечением этелкальцетидом на основании доказательных данных и оценки причинно-следственной связи, перечислены ниже согласно следующей классификации: очень часто (> 1/10); часто (> 1/100 до < 1/10); нечасто (> 1/1,000 до < 1/100); редко (> 1/10,000 до < 1/1,000); очень редко (< 1/10,000).
1 см. раздел «Описание отдельных нежелательных реакций».
2 Термин «гиперкалиемия» включал такие предпочтительные термины, как гиперкалиемия и увеличение концентрации калия в крови.
3 Термин «парестезии» включал такие предпочтительные термины, как парестезия и гипестезия.
Описание отдельных нежелательных реакций
Гипокальциемия
В программе клинических исследований препарата Парсабив бессимптомное снижение концентрации кальция ниже 7.5 мг/дл или бессимптомное снижение концентрации альбумин-корригированного кальция в диапазоне от 7,5 до 8,3 мг/дл, которое требовало лечения или которое исследователь определял как клинически значимое, регистрировалось как «снижение концентрации кальция в крови». Снижение концентрации альбумин-корригированного кальция ниже 8,3 мг/дл, сопровождающееся клиническими проявлениями, регистрировалось как «гипокальциемия» с указанием соответствующих объективных и субъективных симптомов. Большинство событий, представленных бессимптомным снижением концентрации кальция в крови и гипокальциемией с клиническими проявлениями, были легкой или умеренной степени тяжести. В объединенных данных плацебо-контролируемых исследований в группе лечения препаратом Парсабив по сравнению с группой плацебо была выше доля пациентов, у которых, по меньшей мере, однократно регистрировалась концентрация альбумин-корригированного кальция в сыворотке крови < 7,0 мг/дл (7,6% — в группе лечения; 3,1% — в группе плацебо). < 7,5 мг/дл (27,1% — в группе лечения; 5,5% — в группе плацебо) и < 8,3 мг/дл (78,6% — в группе лечения; 19,4% — в группе плацебо). В этих исследованиях 1% пациентов в группе лечения препаратом Парсабив и 0% пациентов группе плацебо прекратили лечение из-за нежелательного явления «низкая концентрация кальция в сыворотке крови».
Удлинение интервала QTc, обусловленное гипокальциемией
В объединенных данных плацебо-контролируемых исследований в группе лечения препаратом Парсабив по сравнению с группой плацебо была выше доля пациентов с максимальным удлинением интервала QTcF более 60 мсек относительно исходного уровня (1,2% — в группе лечения препаратом Парсабив, 0% — в группе плацебо). Доля пациентов, у которых после исходного обследования было зарегистрировано максимальное значение QTcF > 500 мсек (измерение проводилось перед процедурой диализа), составила в группе лечения 4,8%, а в группе плацебо — 1,9%.
Декомпенсация хронической сердечной недостаточности
В совокупности плацебо-контролируемых исследований доля пациентов, у которых наблюдалась декомпенсация хронической сердечной недостаточности, потребовавшее госпитализации, составила 2,2% в группе лечения препаратом Парсабив и 1,2% в группе плацебо.
Отсутствуют клинические данные о передозировке препарата Парсабив. Пациентам, получавшим диализ, препарат вводили в однократной дозе до 60 мг или в многократной дозе до 22,5 мг 3 раза в неделю в конце процедуры диализа. Передозировка препарата Парсабив может привести к гипокальциемии с клиническими проявлениями или без них и может потребовать лечения. Хотя Парсабив выводится при диализе, не проводилось изучение гемодиализа в качестве терапии передозировки препарата Парсабив. С целью своевременного проведения соответствующих вмешательств, при передозировке необходимо контролировать сывороточную концентрацию кальция и наблюдать пациента для выявления симптомов гипокальциемии (см. раздел «Способ применения и дозировка»).
ВЗАИМОДЕЙСТВИЯ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ СРЕДСТВАМИ
Отсутствуют данные о фармакокинетических лекарственных взаимодействиях этелкальцетида. In vitro этелкальцетид не подавлял и не индуцировал активность изоферментов системы цитохромов CYP450, и не являлся их субстратом. In vitro этелкальцетид не являлся субстратом эффлюксных белков-транспортеров и белков-транспортеров захвата (Р-гликопротеина (Pgp), белка резистентности рака молочной железы (BCRP), транспортера органических анионов (ОАТ) 1 и 3, полипептида транспортера органических анионов (ОАТР) 1В1 и 1ВЗ, транспортера органических катионов (ОСТ) 2, транспортера пептидов (РЕРТ) 1 и 2). In vitro этелкальцетид также не демонстрировал способность ингибировать распространенные белки-транспортеры (Pgp, BCRP. ОАТ1, ОАТЗ, ОАТР1В1, ОАТР1ВЗ, ОСТ2 или экспортирующую помпу солей желчных кислот (ЭПЖК)).
Другие лекарственные средства, снижающие концентрацию кальция
Одновременное применение других лекарственных средств, снижающих концентрацию кальция в сыворотке крови, и препарата Парсабив может привести к повышению риска развития гипокальциемии (см. раздел «Особые указания»).
Гипокальциемия
Препарат Парсабив снижает сывороточную концентрацию кальция и может привести к развитию гипокальциемии (см. раздел «Побочное действие»). Лечение препаратом Парсабив не следует начинать у пациентов с ХПН, находящихся на гемодиализе, при концентрации альбумин-корригированного кальция в сыворотке крови ниже нижнего предела нормальных значений (см. раздел «Противопоказания»).
Следует наблюдать за пациентом для выявления гипокальциемии. Контроль концентрации кальция в сыворотке крови следует осуществлять перед началом терапии, в течение одной недели после начала терапии или коррекции дозы, а также каждые 4 недели лечения препаратом Парсабив (см. раздел «Способ применения и дозировка»). Возможные клинические проявления гипокальциемии включают парестезии, миалгии, мышечные спазмы и судороги. Пациенту следует рекомендовать обратиться к врачу в случае появления симптомов гипокальциемии. При клинически значимом снижении концентрации альбумин-корригированного кальция в сыворотке крови необходимо провести мероприятия, направленные на повышение концентрации кальция в сыворотке крови (см. раздел «Способ применения и дозировка»).
Желудочковая аритмия и удлинение интервала QT, обусловленное гипокальциемией
Снижение концентрации кальция в сыворотке крови может привести к удлинению интервала QT, что, в свою очередь, может сопровождаться развитием желудочковой аритмии. У пациентов с врожденным синдромом удлинения интервала QT, удлинением интервала QT в анамнезе, удлинением интервала QT или внезапной сердечной смертью в семейном анамнезе, а также другими состояниями-предикторами удлинения интервала QT и развития желудочковой аритмии необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения препаратом Парсабив.
Судороги
Порог судорожной готовности может быть снижен при значительном уменьшении концентрации кальция в сыворотке крови. У пациентов с судорожными расстройствами в анамнезе необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения препаратом Парсабив.
Декомпенсация хронической сердечной недостаточности
Снижение функции миокарда, гипотензия и хроническая сердечная недостаточность могут быть связаны со значительным уменьшением концентрации кальция в сыворотке крови. У пациентов с хронической сердечной недостаточностью в анамнезе (которая может ассоциироваться с уменьшением концентрации кальция в сыворотке крови) необходимо обеспечить тщательный контроль концентрации кальция в сыворотке крови во время лечения препаратом Парсабив.
Одновременное применение с другими лекарственными средствами
Пациентам, получающим препарат Парсабив, не следует назначать цинакальцет (см. раздел «Способ применения и дозировка»). Их одновременное применение может привести к развитию тяжелой гипокальциемии.
Препарат Парсабив следует с осторожностью назначать пациентам, получающим любые другие лекарственные средства, снижающие концентрацию кальция в сыворотке крови. Пациентам, получающим другие лекарственные средства, которые снижают концентрацию кальция в сыворотке крови, следует обеспечить тщательный контроль этого показателя.
Адинамическая болезнь кости
При длительном подавлении концентрации ПТГ ниже 100пг/мл возможно развитие адинамической болезни кости. При снижении концентрации ПТГ ниже рекомендуемого целевого диапазона необходимо уменьшить дозы или отменить терапию стероловыми формами витамина Д и/или препаратом Парсабив. После отмены терапию возобновляют в более низких дозах для поддержания концентрации ПТГ в пределах диапазона целевых значений (см. раздел «Способ применения и дозировка»).
Особые группы пациентов
Дети
У детей безопасность и эффективность препарата Парсабив не установлена.
Пожилые пациенты
Отсутствовали клинически значимые различия безопасности и эффективности между пациентами в возрасте 65 лет и старше и пациентами более молодого возраста (> 18 и <65 лет). Не были обнаружены различия концентрации этелкальцетида в плазме крови между пациентами в возрасте 65 лет и старше и пациентами более молодого возраста (> 18 и < 65 лет). Из 503 пациентов, получавших препарат Парсабив в плацебо-контролируемых исследованиях, 177 пациентов (35,2%) были в возрасте 65 лет и старше.
Печеночная недостаточность
Этелкальцетид не подвергается печеночному метаболизму; поэтому ожидается, что печеночная недостаточность не будет оказывать значительного эффекта на выведение этелкальцетида. Влияние печеночной недостаточности на фармакокинетику этелкальцетид не изучалось (см. раздел «Фармакокинетика»).
Почечная недостаточность
Парсабив показан пациентам, находящимся на гемодиализе. Влияние степени тяжести почечной недостаточности на фармакокинетику препарата Парсабив не изучено (см. раздел «Фармакокинетика»).
Иммуногенностъ
Оценка иммуногенности этелкальцетида проводилась с помощью иммунологического исследования на основе поверхностного плазмонного резонанса, которое позволяло обнаружить связывающие антитела к этелкальцетиду. В клинических исследованиях у 7.1% (71 из 995) пациентов с вторичным гиперпаратиреозом (ГПТ), получавших лечение этелкальцетидом в период до 6 месяцев, обнаруживались связывающие антитела (при этом у 80,3% из них [у 57 из 71] антитела были выявлены при исходном обследовании).
Не отмечено изменения фармакокинетического профиля, клинического ответа или профиля безопасности, вызванных наличием антител к этелкальцетиду, изначально присутствовавших, или выработанных во время лечения. При подозрении на образование антител к этелкальцетиду, которое сопровождается клинически значимыми эффектами, пожалуйста, свяжитесь с компанией «Амджен» для решения вопроса о проведении лабораторного исследования для выявления антител.
Особые указания по применению и меры предосторожности
Препарат Парсабив не требует смешивания или разведения перед применением. Раствор является прозрачным и бесцветным. Перед применением препаратов для парентерального введения необходимо предварительно произвести визуальный осмотр для выявления инородных частиц и изменения цвета. Раствор нельзя применять при помутнении или изменении цвета, содержании мутных или окрашенных включений.
ВЛИЯНИЕ НА СПОСОБНОСТЬ УПРАВЛЯТЬ ТРАНСПОРТНЫМИ
СРЕДСТВАМИ И МЕХАНИЗМАМИ
Исследования влияния препарата Парсабив на способность управлять транспортными средствами и механизмами не проводились.
Раствор для внутривенного введения 2,5 мг/ 0,5 мл, 5,0 мг/1 мл, 10 мг/ 2 мл.
По 0,5 мл, 1,0 мл или 2,0 мл раствора во флаконе объемом 3 мл из стекла гидролитического класса с эластомерной пробкой, ламинированной фторполимером, алюминиевым колпачком и отламывающимся полипропиленовым колпачком.
6 флаконов помещают в пачку картонную вместе с инструкцией по применению. На каждую пачку наклеивают защитные этикетки — контроль первого вскрытия, имеющие продольную цветную полосу.
Хранить при температуре от 2°С до 8°С. Не замораживать.
Хранить в оригинальной упаковке для защиты от света.
Не встряхивать.
Хранить в недоступном для детей месте!
При изъятии из холодильной камеры возможно хранение лекарственного препарата при температуре не выше 25°С в течение 7 дней в оригинальной упаковке (картонной пачке), в случае хранения флакона без картонной пачки — в течение 4 часов, избегая воздействия прямых солнечных лучей.
2 года.
Не применять по истечении срока годности, указанного на упаковке.
Отпускают по рецепту.
ЮРИДИЧЕСКОЕ ЛИЦО, НА ИМЯ КОТОРОГО ВЫДАНО
РЕГИСТРАЦИОННОЕ УДОСТОВЕРЕНИЕ
«Амджен Европа Б.В.» Минервум 7061 4817 ZK Бреда Нидерланды
ПРОИЗОДИТЕЛЬ, ОСУЩЕСТВЛЯЮЩИЙ выпускающий контроль КАЧЕСТВА
«Амджен Европа Б.В.» Минервум 7061 4817 ZK Бреда Нидерланды
ПРЕДСТАВИТЕЛЬ В РОССИЙСКОЙ ФЕДЕРАЦИИ
ООО «Амджен»
123317, Москва, Пресненская наб., дом 8, корпус 1; 7-й этаж